Comments
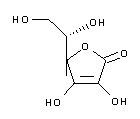
Una función importante del ácido ascórbico (vitamina C) en el organismo es la protección del Fe2+ en las oxigenasas de la oxidación a Fe3+ o como agente reductor en las reacciones de hidroxilación, como la conversión de prolina a hidroxiprolina en el colágeno. El ácido ascórbico en solución acuosa se oxida de forma irreversible por el oxígeno atmosférico a ácido L-dicetogulónico y otras sustancias biológicamente inactivas. Para la preparación de cloroplastos, se utilizan los agentes reductores fisiológicos ácido ascórbico y glutatión (3, 4). La solución madre de ascorbato (100X) se compone de 50 mM de HEPES-NaOH (pH 7,6) con 0,5 M de ascorbato y se almacena a -20°C. La concentración de trabajo es de 2 mM (4) a 5 mM (3) de ascorbato.
Literature
(1) Kanfer, J.N. & Spielvogel, C.H. (1973) Biochim. Biophys. Acta 327, 405-411. Inhibición de la β-N-acetilhexosaminidasa por las lactonas. (2) Omaye, S.T. et al. (1979) Methods Enzymol. 62, 3-11. Métodos para la determinación de de ácido ascórbico en células, tejidos y fluidos animales. (3) Gegenheimer, P. (1990) Methods Enzymol. 182, 174-193. Preparación de extractos de plantas. (4) Hager-Braun, C. et al. (1995) Biochemistry 34, 9617-9624. Photobleaching estable de P840 en preparaciones del centro de reacción de Chlorobium: presencia de la proteína de bacterioclorofila a de 42 kDa y de un polipéptido de 17 kDa.